¿Son peligrosas las manicuras en gel?

Artículo publicado en The New York Times el 22 de febrero de 2023
IDONEIDAD, HONESTIDAD, VOCACIÓN DE SERVICIO

Artículo publicado en The New York Times el 22 de febrero de 2023

La pandemia por COVID-19, causada por el SARS-CoV-2, ha transformado la vida cotidiana en todo el planeta. Hasta el 6 de abril de 2020, la enfermedad se había extendido a más de 210 países y territorios, con más de 1,2 millones de casos y 67.594 muertes reportadas. En respuesta, la mayoría de los gobiernos implementaron medidas de distanciamiento social con el objetivo de frenar la propagación del virus y minimizar su impacto sanitario.
Uno de los cambios más significativos fue el cierre masivo de escuelas: 188 países interrumpieron la educación presencial, dejando a más de 1.500 millones de estudiantes fuera del aula. Sin embargo, la evidencia científica sugiere que esta medida, si bien preventiva, tiene beneficios limitados frente a los costos sociales, educativos y emocionales que genera.
Un modelo realizado por Ferguson y su equipo en el Reino Unido estimó que el cierre de escuelas reduciría la mortalidad por COVID-19 en apenas un 2–4%. Esta cifra cobra aún más relevancia si consideramos que, a diferencia de lo que sucedió durante la pandemia de gripe H1N1 en 2009, el coronavirus afecta en menor medida a niños y adolescentes, quienes en su mayoría cursan la infección de manera leve o asintomática.
Una revisión sistemática publicada el 6 de abril de 2020 por Russell Viner y colaboradores, que analizó 16 estudios sobre cierres escolares en China, Hong Kong y Singapur, concluyó que el impacto sobre la transmisión viral fue limitado. Los autores destacaron la necesidad de valorar esta medida dentro de un contexto más amplio, considerando sus múltiples efectos colaterales.
El impacto del cierre de escuelas va mucho más allá de lo académico. En contextos de bajos ingresos, las escuelas no solo educan: también proporcionan servicios de salud, alimentación, higiene y protección. El confinamiento forzado ha generado:
En África Occidental, tras la epidemia de ébola, se registró un aumento de trabajo infantil, abuso sexual, embarazos adolescentes y deserción escolar. Este precedente alerta sobre los riesgos que la interrupción prolongada de la escolaridad puede acarrear.
La adolescencia es una etapa clave para la construcción de identidad y la conexión con los pares. La suspensión de actividades presenciales, sumada a la incertidumbre por exámenes y futuros truncos, genera ansiedad, frustración y un sentido de pérdida en muchos jóvenes.
Además, la pandemia ha privado a muchos adolescentes de vivir experiencias fundamentales como las ceremonias de graduación, viajes de fin de curso o primeros empleos, elementos que marcan transiciones significativas en la vida personal y social.
Los gobiernos deben priorizar la reapertura segura y progresiva de las escuelas, contemplando estrategias como horarios reducidos, clases alternadas o modalidades híbridas. Será crucial acompañar emocionalmente a los estudiantes en el retorno, especialmente a aquellos que hayan atravesado situaciones de duelo, violencia o privaciones.
Pese a las dificultades, la pandemia también reveló la capacidad de los jóvenes para adaptarse, liderar y aportar. Historias como la de Xian Lu, quien se trasladó a Wuhan para cocinar 400 comidas diarias para el personal médico, simbolizan una juventud empática y comprometida.
La enviada especial para la Juventud del Secretario General de la ONU, Jayathma Wickramanayake, reconoció a Xian Lu y otros jóvenes por su labor comunitaria durante la pandemia. Este tipo de acciones demuestra que, en medio de la crisis, muchos adolescentes están desarrollando valores fundamentales como la responsabilidad social, el altruismo y la solidaridad.
Aunque el SARS-CoV-2 rara vez cause formas graves en niños y adolescentes, los impactos sociales, psicológicos y educativos del COVID-19 pueden ser profundos y duraderos. Por eso, es fundamental escuchar a los jóvenes, validar sus emociones y acompañarlos en el desarrollo de habilidades que los preparen para un futuro incierto pero también lleno de oportunidades.
La pandemia nos obliga a repensar los sistemas educativos, de salud y protección infantil, con un enfoque más inclusivo, equitativo y centrado en las verdaderas necesidades de los más jóvenes.


Los ejercicios de equilibrio mejoran la capacidad para controlar y estabilizar la posición del cuerpo. Este tipo de ejercicio es particularmente importante para los adultos mayores ya que a medida que se envejece, empeora la capacidad para saber cómo se encuentra nuestro cuerpo en el espacio (propiocepción), lo que contribuye a una disminución del equilibrio, según Kelly Drew, fisiólogo de ejercicio en American College of Sports Medicine

Más allá de lo conveniente que es en los adultos mayores este tipo de entrenamiento, los ejercicios de equilibrio pueden beneficiar a personas de cualquier edad, incluso las personas que han ganado o perdido mucho peso o que están embarazadas, por lo que puede haber cambiado su centro de gravedad.
Estos ejercicios también son importantes para reducir el riesgo de lesiones. Por ejemplo, cuando se sufre un esguince de tobillo, se puede estar en riesgo de una nueva lesión si no se ejercita el equilibrio, según el Dr. Edward Laskowski, co-director de la Mayo Clinic Sport Medicine Center, de Rochester, Minnesota. Esto puede ocurrir, porque cuando se sufre un esguince de tobillo, los músculos alrededor de la articulación no se contraen de manera coordinada y desestabiliza la articulación. Si se hace ejercicios de equilibrio después de la lesión, se vuelve a entrenar los músculos para que se contraigan juntos, lo que mejora la estabilidad de la articulación durante los movimientos y evita nuevas lesiones,

La mayoría de los atletas pueden beneficiarse del entrenamiento del equilibrio que les ayuda a mantener mejor la coordinación durante la actividad deportiva. «En casi todos los esfuerzos atléticos, se puede a estar en un pie a la vez, mientras que están haciendo las cosas», dice, Jason Schatzenpahl, un especialista en acondicionamiento físico en el Centro de Salud y Bienestar CU Anschutz en Aurora, Colorado.
Ejemplos de ejercicios de equilibrio incluyen:
Ventajas de hacer ejercicio de equilibrio incluyen:
¿Cuánto ejercicios para el equilibrio se necesitarían?
No hay límite a la cantidad de equilibrio de formación puede hacerlo con seguridad – usted puede hacerlo todos los días si quieres, según Laskowski. Un estudio de revisión del 2015 encontró que el hacer de tres a seis sesiones de entrenamiento del equilibrio por semana, con cuatro ejercicios de equilibrio por sesión de entrenamiento, de 11 a 12 semanas fue eficaz para mejorar el equilibrio de las personas.
¿Cómo se puede evitar lesiones cuando se hace ejercicios de equilibrio?
El principal riesgo de hacer ejercicios de equilibrio son las caídas. Hay que asegurarse de tener algo cercano a la que se puedan aferrarse si se desequilibran, según Drew. Si se utiliza un equipo como tableros de estabilidad, debe asegurarse que está en una superficie plana, estable y antideslizante, de acuerdo con el American College of Sports Medicine.
Comenzar con ejercicios de equilibrio sencillos, como desplazar el peso de lado a lado o de pie en un pie durante unos segundos, y poco a poco hacer que sus sesiones más difíciles – por ejemplo, aumentando el tiempo que pasa en un pie, el ACSM recomienda. También, se debe comenzar en superficies estables y en una sola posición antes de añadir cualquier movimiento o equipo de ejercicio de equilibrio.
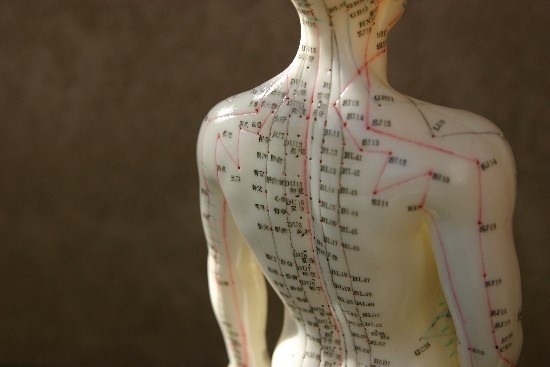
La acupuntura es un tratamiento que data de alrededor del 100 a C en China. Se basa en conceptos chinos tradicionales como qi (pronunciado «chee» y energía de fuerza de vida considerada) y meridianos (rutas a través de las cuales fluye el qi). Múltiples estudios no han podido demostrar alguna evidencia científica que respalde dichos principios. La acupuntura implica la inserción de agujas delgadas en la piel en ubicaciones múltiples y variables según los síntomas del paciente. Una vez insertadas, algunos acupunturistas le dan la vuelta a las agujas para obtener un beneficio terapéutico adicional. Aunque hay muchos usos para la acupuntura en la medicina tradicional china, en la medicina occidental se usa principalmente para el tratamiento del dolor.
En un momento en que muchas personas están cada vez más preocupadas por los efectos secundarios de los medicamentos, algunos consideran que la acupuntura es una opción atractiva que no requiere medicamentos. Desafortunadamente, muchos estudios muestran que los beneficios potenciales de la acupuntura son de corta duración. En mi experiencia, puse la acupuntura, el masaje y las intervenciones quiroprácticas en el mismo cubo. Puede sentirse mejor por un día o dos, pero hay una mejora duradera limitada.
En un estudio , 249 personas con migrañas que ocurrían de dos a ocho veces al mes recibían acupuntura, acupuntura simulada (falsa / placebo), o eran incluidas en una lista de espera de acupuntura. Los dos grupos de tratamiento recibieron tratamiento cinco días a la semana durante cuatro semanas. Doce semanas después del tratamiento, el grupo de acupuntura tuvo un promedio de 3.2 ataques menos por mes, el grupo simulado de acupuntura tuvo 2.1 ataques menos por mes y el grupo de lista de espera tuvo 1.4 ataques menos por mes. Estos resultados son modestos en el mejor de los casos, y tienen un costo de tratamiento aproximado de US$ 2,000 por mes (estimando US$ 100 / sesión x 20 sesiones). Esta cifra no incluye los ingresos perdidos por el tiempo fuera del trabajo para asistir a las citas, los costos de viaje, el dolor del procedimiento y el tiempo de recuperación.
En general, la efectividad del tratamiento estándar (medicamentos y terapias inyectables) está respaldada por una evidencia científica mucho más sólida que la acupuntura, que incluye grandes ensayos clínicos con miles de sujetos. Para aquellos reacios a los medicamentos, la terapia física es una gran alternativa, una basada en la anatomía humana real y los principios científicos. Mis pacientes a menudo se quejan de que no se sienten significativamente mejor después de las cinco a diez sesiones de terapia física que las compañías de seguros generalmente aprueban. Les aconsejo que el verdadero beneficio de la terapia física se produce cuando las rutinas de estiramiento y fortalecimiento enseñadas por el terapeuta se continúan en el hogar a largo plazo. Esperar una cura instantánea y permanente de la terapia física es como ir al gimnasio por una semana, y esperando perder 20 libras, sin ninguna posibilidad de recuperar el peso. (Si algún lector encuentra un gimnasio así, hágamelo saber …)
A un costo de alrededor de US$ 100 por tratamiento, y con sesiones que pueden durar más de una hora, los tratamientos de acupuntura pueden estar limitados tanto por el tiempo como por el costo. Algunos pacientes pueden afirmar con confianza que no les importa el costo, ya que su plan de seguro cubre la acupuntura. Advertiría a esos mismos pacientes que el dinero no crece en los árboles, especialmente en el bosque de seguro médico. Si el dinero se gasta en un gasto, no se puede gastar en otra cosa. Un plan que cubre la acupuntura puede incluir letra pequeña sobre copagos excesivos o cobertura limitada para medicamentos básicos. En algunos casos, cubrir la acupuntura o el masaje puede afectar a otros pacientes en el mismo grupo. Imagínese si todos recibieran masajes gratis, pero a su vez la quimioterapia que salva vidas de un paciente con cáncer se vuelve inalcanzable. Aunque este es un ejemplo exagerado,
Los efectos secundarios no se limitan solo a los medicamentos; los procedimientos también pueden tener efectos negativos. La acupuntura es relativamente segura cuando el médico utiliza agujas estériles de un solo uso con una técnica limpia. Los efectos secundarios pueden incluir infecciones de la piel, sangrado y neumotórax (pulmón colapsado) si las agujas se insertan demasiado profundamente en el pecho. Los médicos a veces realizan acupuntura, pero no se requiere capacitación médica, y las calificaciones para obtener una licencia para practicar acupuntura varían según el estado. Probablemente valga la pena el gasto adicional para tener un acupunturista más experimentado y / o con más credenciales.
The Long-term Effect of Acupuncture for Migraine Prophylaxis, A Randomized Clinical Trial. JAMA Internal Medicine, 2017.
Harvard Health Publishing – HARVARD MEDICAL SCHOOL
Paul G. Mathew, MD, FAAN, FAHS
Contribuidor

A raíz de acontecimientos recientes donde un niño de solo 7 años murió supuestamente de desnutrición, tuberculosis y Chagas, en los medios se mostró teóricamente, un certificado de defunción donde no se especificaba de manera clara, la causa de fallecimiento. Esto vuelve poner en la palestra la metodología con que los médicos argentinos confeccionan el certificado médico de defunción (CMD).
En relación al certificado médico que volvió a levantar la polvareda, fue un certificado que se mostró en algunos periódicos de los primeros días de enero de 2015, el cual se fotocopia a continuación (figura 1).
 El documento publicado, de hecho, no es un certificado de defunción oficial, realizado por un médico. En primer lugar, porque cuando coloca la causa de muerte solo asienta la palabra “Enfermedad”, sin mencionar ninguna lesión responsable del deceso. En segundo lugar está firmado supuestamente por el padre del niño (Claudio Femenias) y no existe CMD firmado por un no médico o un familiar.
El documento publicado, de hecho, no es un certificado de defunción oficial, realizado por un médico. En primer lugar, porque cuando coloca la causa de muerte solo asienta la palabra “Enfermedad”, sin mencionar ninguna lesión responsable del deceso. En segundo lugar está firmado supuestamente por el padre del niño (Claudio Femenias) y no existe CMD firmado por un no médico o un familiar.
No vamos a entrar en la polémica si hay o no orden de algunos gobernantes, de ocultar ciertas enfermedades como causas de muerte, lo que he visto durante todos los años de mi carrera profesional en la actividad estatal, es que en primer lugar los médicos de instituciones públicas, no son tan sumisos, que si bien como en toda la población hay obsecuentes, la mayoría de ellos se sienten muy tranquilos por su estabilidad laboral y no aceptan presiones que los obliguen a faltar a sus responsabilidades profesionales o realizar cosas que no quieren hacer y mucho menos de manera gratuita. Lo que si creo es que muchas veces, por desconocimiento de la relevancia médico legal de la emisión de dicho documento, la subestimación de la importancia estadística del diagnóstico como causa de muerte o simplemente por negligencia, se ha usado y abusado de términos que no explican exactamente las enfermedades que causaron la muerte, p. e. paro cardiorrespiratorio
Como es conocido, la palabra certificado, del verbo certificar, viene del latín, “certificare” que significa: asegurar, afirmar, dar por cierto algo, que en manos médica siempre se refiere a temas de salud y en este caso particular asegura que un ser humano nacido vivo, no tiene vida al momento del examen del profesional, con toda la implicancia legal, judicial y estadística que esto significa.
No hay que confundir la certificación de la muerte de un ser humano con el CMD. Lo primero certifica exclusivamente la falta de signos vitales en un individuo, sin especificar la causa del mismo y todos los médicos estamos obligados a realizarlo, cuando somos llamados a la hora que sea por este motivo. Por otro lado, el CMD, certifica más allá del fallecimiento, el diagnóstico de las enfermedades que llevaron el proceso hacia la muerte, este último certificado, no todos los médicos están obligados ni habilitados a realizar, solo aquellos que conocen de manera efectiva, los procesos patológicos que concluyeron con la vida del paciente. Por ejemplo, puede ocurrir que los convivientes y/o allegados de un convaleciente, llamen a un servicio de emergencia médica por considerar que este ha fallecido; estos galenos, efectivamente certifiquen las falta de signos vitales pero se nieguen a confeccionar el CMD por no conocer al paciente ni los antecedentes médicos del mismo y se deba convocar al medico de cabecera o al medico de familia y de no disponer de ellos, debería realizársele una autopsia que permitiría establecer la causa cierta de la muerte.
Como es conocido por todos, hay dos tipos básicos de diagnósticos de muerte, por causa naturales y no naturales (causas judiciales). Causas naturales son todas aquellas muertes devenidas de procesos patológicos internos: infecciones, cánceres, cardiopatías, neumopatías etc.. Las causas no naturales o judiciales son aquellas muertes por causas externas, entre ellas podemos mencionar: accidentes (domésticos, laborales, de tránsito, etc.) o criminales (homicidios, suicidios, envenenamientos, lesiones por armas blancas, armas de fuego, etc.).
No es objeto de este informe, la confección del CMD de las causas de muerte judiciales, que en general son patrimonio de los médicos forenses, sino que el objetivo es exclusivamente, revisar los diagnósticos utilizados por los médicos asistenciales, en la elaboración del CMD, cuando la muerte ocurre por causas NATURALES.
Hay dos premisas que quisiera remarcar sobre el CMD, por un lado, no es una urgencia médica, es decir, que si ya se conoce que el paciente a muerto y si se llama al médico de cabecera para que firme el CMD, este puede terminar con los turnos del consultorio y recién concurrir al domicilio del fallecido a confeccionar el certificado. En segundo lugar, que ningún médico está obligado a realizarlo, si no conoce exactamente la causa de muerte, por no haber intervenido en el tratamiento de la enfermedad que llevó al paciente al deceso o no disponer de documentación confiable al respecto.
En los casos en que el médico está habilitado a la confección del certificado, porque es el médico de cabecera, porque participó del proceso de éxitus, porque dispone de documentación fiable, porque el cadáver no presenta ningún signo de muerte judicial, etc., etc., hay que cumplir con las formalidades protocolares, llenando el formulario oficial para este fin, que en líneas generales, sigue las instrucciones de la OMS (World Health Organization, 1980. publicación nº: 924356062X) (figura 2).
Los diagnósticos que se deberían usar para llenar este formulario son los que se encuentran codificados en la Décima Clasificación Internacional de las Enfermedades (CIE 10). Cabe recordar que una de las raíces históricas de la CIE 10, en el siglo XII, fue la Lista Internacional de Causas de Muertes, que los médicos fueron implementando, para conocer de qué se morían las personas y poder actuar en consecuencia. A pesar de las imperfecciones de esas primitivas listas, eran tan evidentes las ventajas a la hora de protocolizar las estadísticas médicas, que se decidió ampliar el listado a todas las causas de morbilidad creándose la “Clasificación Internacional de Causas de Enfermedad y Muerte” (CIE). Cuando en 1948 se creó la 1ª Asamblea Mundial de Salud, (OMS), se le solicitó a esta organización que se hiciera cargo de la revisión, planificación y actualización del listado, dando origen a la CIE. Es decir que este listado codificado, nació, en un principio, para protocolizar estadísticamente las causas de muerte, es por esto, que es de relevancia que se emplee esta clasificación para llenar el formulario de CMD, que permite unificar mundialmente la denominación médica estadística.
Volviendo a la confección del formulario oficial del CMD, se puede ver que en el primer punto, «Causas de defunción», tiene dos ítems, el primero, I a), es para asentar la causa última o directa de la muerte, pero como bien se indica en el asterisco, no es para colocar el mecanismo de la muerte, por ejemplo “paro cardiorespiratorio”, sino se debe colocar “la enfermedad, lesión o complicación que causó el fallecimiento”, por ejemplo shock cardiogénico, infarto de miocardio, neumonía, edema agudo de pulmón, etc.. Quisiera insistir en el concepto, en que no se debe usar como causa directa de muerte, el término «PARO CARDIORRESPIRATORIO»; este término no está codificado en el CIE 10, no es una causa de muerte y podríamos decir más precisamente, que es una consecuencia de la muerte.
En el punto I b) y I c) (y las letras sucesivas si fueran necesarios), se debe asentar cuando la causa directa de la muerte (I a) es a consecuencia de una segunda patología y esta a su vez de una tercera, p. e. I a): Accidente Cerebrovascular, debido a I b): Hipertensión Arterial
Puede suceder que la lesión o patología que causó directamente la muerte, no sea debido a ninguna otra causa y por lo tanto en los ítems I b) y c) no consignarse nada, p e: I a): Neumonía de la comunidad.
En el punto II, se debe asentar, si existiera, otra patología que pudo haber contribuido de alguna manera a la causa de muerte pero no de manera directa, p e: I. a) Asfixia por vómito; I. b) Accidente Cerebrovascular; I c) Hipertensión Arterial y en II: Insuficiencia Cardíaca Congestiva. Por último en la columna de la derecha, debe asentarse el tiempo trascurrido desde el diagnóstico de las patologías mencionadas hasta la muerte.
En relación al niño Feminas, si bien no se conoce públicamente la historia clínica evolutiva de las patologías del niño y solo en el campo de las suposiciones podríamos decir que: el niño debido a su desnutrición tenía una la disminución de sus defensas inmunológicas que facilitó la infección tuberculosa que le ocasionó la muerte. Esta condición se vio favorecida aparte por una cardiopatía chagásica. Siempre en el campo de las hipótesis, a la hora de completar el certificado médico de defunción, podríamos asentar:
I. a) Infección tuberculosa (A15) 6 meses
I. b) Desnutrición (E43) 7 años
II. Enfermedad de Chagas (E57) 5 años
Sería relevante que aparte del diagnostico médico, se agregara el código correspondiente a la Décima Clasificación Internacional de Enfermedades (CIE 10), para facilitar la elaboración estadística de las causas de muerte en la Argentina, para lo cual, se debe tener en cuenta como tal, la patología mencionada en el último punto del ítem I. Considerando el caso del niño que nos convoca, si la hipótesis se confirmara, sería la Desnutrición (E43) la causa efectiva de muerte.
A manera de conclusión, diría que no se debería aceptar administrativamente, nunca mas, un CMD que asiente como causa de muerte, PARO CARDIORRESPIRATORIO.
BIBLIOGRAFIA
La Medicina Legal es una disciplina que aplica los conocimientos médicos y científicos al ámbito jurídico. Su objetivo es esclarecer hechos de relevancia legal, proporcionando pruebas y análisis que ayuden a la administración de justicia. Es una rama fundamental en la investigación de delitos y en la evaluación de daños corporales, responsabilidad médica y otros aspectos legales relacionados con la salud.
La Medicina Legal tiene múltiples aplicaciones en el ámbito judicial y médico. Algunas de sus principales funciones incluyen:
La Medicina Legal abarca diversas áreas de especialización, entre las cuales se destacan:
La Medicina Legal es una disciplina esencial en la administración de justicia, ya que permite esclarecer hechos, descartar simulación y disimulación, determinar responsabilidades y garantizar la protección de los derechos humanos. Su integración con la ciencia y el derecho la convierte en un pilar fundamental para la resolución de conflictos legales con base en la evidencia científica.

Las Directivas Médicas Anticipadas (DMA) son una herramienta legal y ética que permite a toda persona expresar, de forma escrita, qué tipo de atención médica desea o no desea recibir en caso de que en el futuro no pueda tomar decisiones por sí misma debido a una enfermedad grave, discapacidad o pérdida de conciencia.
Son, en esencia, una manera de garantizar la autonomía personal incluso en situaciones de incapacidad. También alivian a las familias y profesionales de salud al ofrecer una guía clara sobre los deseos del paciente.
En Argentina, las Directivas Médicas Anticipadas están reguladas por la Ley 26.529, modificada por la Ley 26.742 (Ley de Muerte Digna). Esta normativa establece que:
El Código Civil y Comercial de la Nación (vigente desde 2015) también reconoce estas figuras en sus artículos 59, 60 y 61, consolidando el derecho a la autodeterminación en materia sanitaria.
En Córdoba, las DMA están alineadas con la legislación nacional. El Ministerio de Salud de la Provincia y el Colegio de Médicos reconocen su validez siempre que se cumplan los requisitos formales.
En 2022, el Ministerio de Salud emitió recomendaciones para la implementación de DMA en hospitales públicos, y promueve su registro formal. Aunque no existe un “registro provincial obligatorio”, es recomendable:
Imaginemos a Marta, una mujer de 75 años con diagnóstico temprano de Alzheimer. Antes de que su enfermedad avance, decide redactar una Directiva Médica Anticipada en la que deja claro que, si pierde la conciencia de manera irreversible, no desea ser sometida a respiración mecánica ni alimentación por sonda. Además, designa a su hija como su representante.
Gracias a este documento, en el futuro sus deseos serán respetados, y su familia y médicos podrán actuar con claridad y sin culpa.
Las Directivas Médicas Anticipadas son una herramienta poderosa y aún subutilizada. Promueven el respeto por la dignidad humana y ofrecen seguridad a todas las partes involucradas en la atención médica. En un contexto como el argentino, donde las decisiones en salud suelen ser postergadas o delegadas, promover su uso es un acto de ciudadanía y conciencia ética.
